研究内容
免疫療法のためのTLRリガンドを用いた糖鎖アジュバント (免疫増強剤) の開発
研究背景
アジュバントは、ワクチン抗原と共に投与し、その効果を増強する目的で使用される物質(免疫増強剤)です。ワクチン接種において、抗原分子の投与のみでは十分にワクチン効果が得られない場合が多く、その効果を増強するためにアジュバントが使用されます。近年では、自身の免疫系を活性化させることでがんやアレルギーなどを治療する免疫療法にもアジュバントが使用されるようになり、その応用範囲が拡大しています。一方、現在臨床利用されているアジュバントは、液性免疫(抗体産生)を増強しますが、ウイルスやがんに対する免疫応答に重要な細胞性免疫の誘導能が低いことが課題です。そのため、細胞性免疫を誘導可能な新たなアジュバントの開発が求められています。私たちは、自然免疫を活性化するToll様受容体 (TLR)※1 のリガンドに着目し、TLRリガンドと糖鎖の複合体による新たなアジュバントの開発研究を行っています。
※1 Toll様受容体 (TLR) … ウイルスや細菌などの病原体に特有の分子パターン(PAMP)を認識し、自然免疫を活性化する受容体。ヒトでは10種類が見出されており、病原体の感染を察知するセンサーとして働く。TLRにPAMPが結合すると炎症性サイトカインやI型インターフェロンなどが産生され、自然免疫が活性化される。その後、獲得免疫の誘導が促進されることから、宿主の防御機構において極めて重要な役割を果たしている。このような背景から、TLRを活性化する様々なリガンド分子が開発され、アジュバントとして利用する研究が世界中で活発に行われている。
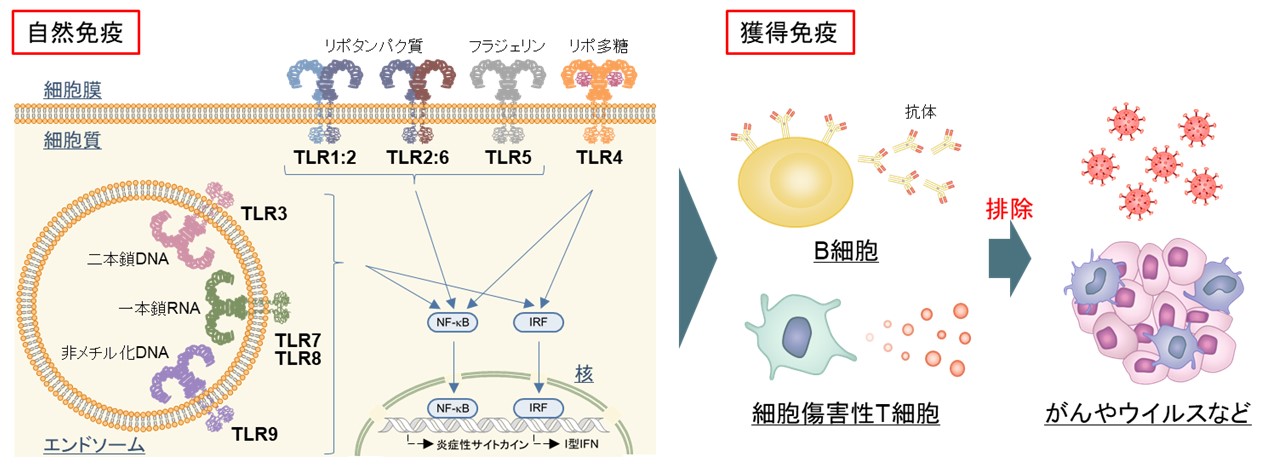
TLR7リガンド・糖鎖固定化金ナノ粒子の開発
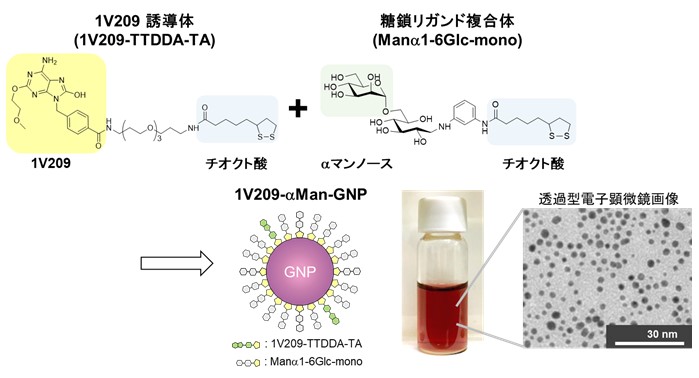
TLR7は主に細胞内のエンドソームに局在し、ウイルス由来の一本鎖RNA (ssRNA) を認識する受容体です。TLR7には低分子化合物が結合することも見出されており、臨床利用が認可されているイミキモド (商品名:ベセルナクリーム) をはじめ、種々の合成低分子リガンドが開発され、アジュバントとしての利用が期待されています。一方、全身投与すると血流で急速に拡散し、サイトカイン放出症候群などの重篤な副作用を引き起こす危険性があるため、その利用法が局所投与に制限されています。これを改善するためには、TLR7リガンドの薬物動態を改善し、効力を強くする必要があります。私たちは、免疫細胞表層に病原体などの外来異物を捕捉するための糖鎖受容体が発現していることに着目し、糖鎖固定化金ナノ粒子 (SGNP) を用いて低分子TLR7リガンドの薬物動態を改善する研究を行っています。つまり、SGNPをキャリヤー分子に用いることで、糖鎖受容体を介してTLR7リガンドを免疫細胞選択的に輸送できるようになり、安全且つ効果的なアジュバントになると期待しています。金ナノ粒子はアジュバント化合物や糖鎖だけでなく、病原体やがんなどの抗原分子も簡便に固定化できるため、ワクチン開発における有用な分子基盤にもなると期待できます。これまでに、合成低分子TLR7リガンドの1V209とα-マンノースを共固定化した金ナノ粒子が細胞性免疫を強く誘導することを見出しており、ワクチンやがん免疫療法のアジュバントとして利用する研究に取り組んでいます。
<関連論文>
Shinchi H., et al., Gold Nanoparticles Coimmobilized with Small Molecule Toll-Like Receptor 7 Ligand and α-Mannose as Adjuvants.
Bioconjugate Chem. 2019, 30(11), 2811-2821. doi.org/10.1021/acs.bioconjchem.9b00560
Shinchi H., Yuki Y., et al., Glyco-Nanoadjuvants: Sugar Structures on Carriers of a Small Molecule TLR7 Ligand Affect Their Immunostimulatory Activities.
ACS Appl. Bio Mater. 2021, 4(3), 2732-2741. doi.org/10.1021/acsabm.0c01639
Shinchi H., Komaki F., et al., Glyco-Nanoadjuvants: Impact of Linker Length for Conjugating a Synthetic Small-Molecule TLR7 Ligand to Glyco-Nanoparticles on Immunostimulatory Effects
ACS Chem. Biol. 2022, 17(4), 957-968. doi.org/10.1021/acschembio.2c00108