研究内容
TLRリガンドを用いたナノ粒子型糖鎖修飾アジュバントの開発
合成低分子TLR7リガンドを用いた糖鎖ナノアジュバント
TLR7は免疫細胞内のエンドソームに存在し、ウイルス由来の一本鎖RNAを感知します。このTLR7が活性化されると、抗ウイルス・抗腫瘍免疫の誘導に重要な炎症性物質 (炎症性サイトカイン、特に I 型インターフェロン) の産生が促進されます。そのため、これまでに多くの合成低分子TLR7リガンドが開発されてきました。代表的な化合物であるイミキモド (商品名:ベセルナクリーム) は、皮膚悪性黒色腫やウイルス性性感染症の治療薬として臨床的に利用されています。一方で、これらの低分子TLR7リガンドを全身投与すると、過剰な炎症性サイトカインの放出により重篤な副反応を引き起こすリスクがあり、ワクチンやがん免疫療法のアジュバントとしての応用は十分に進んでいません。こうした副反応を抑えつつ効果的に免疫を活性化するためには、薬物動態の最適化と投与量の低減が重要な課題とされています。
そこで私たちは、免疫細胞表面に豊富に発現する糖鎖受容体に着目し、糖鎖修飾金ナノ粒子 (SGNP) を低分子TLR7リガンドのキャリアとして用いた『TLR7標的型糖鎖ナノアジュバント』を開発しました。本技術により、低分子TLR7リガンドを標的免疫細胞、特に樹状細胞の細胞内へ選択的かつ効率的に送達することが可能となり、液性免疫および細胞性免疫の双方に対する誘導能が大幅に向上しました。現在、この糖鎖ナノアジュバントを感染症ワクチンおよびがん免疫療法のアジュバントとして応用展開する研究を進めています。
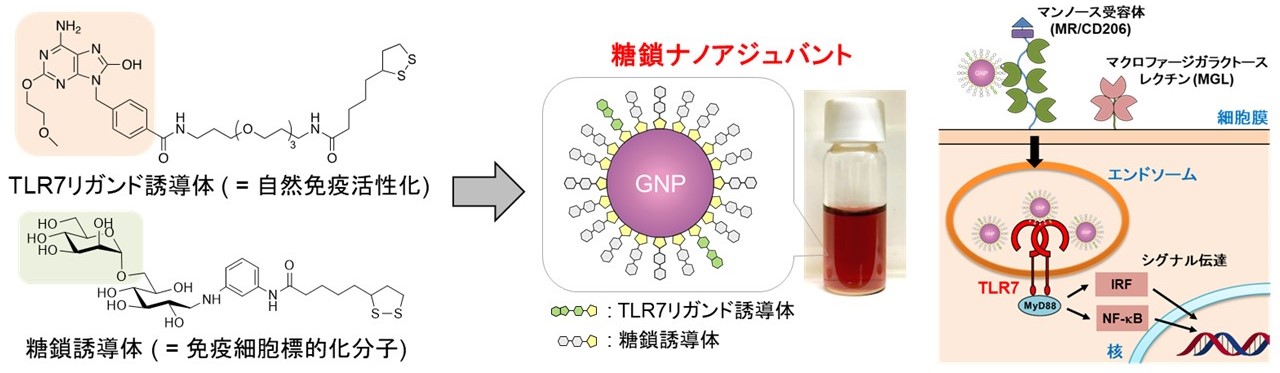
図. TLR7リガンド(1V209)とα-マンノースを固定化した金ナノ粒子
<関連論文・特許>
- Shinchi H., et al., Gold Nanoparticles Coimmobilized with Small Molecule Toll-Like Receptor 7
Ligand and α-Mannose as Adjuvants.
Bioconjugate Chem. 30(11), 2811-2821 (2019)
doi.org/10.1021/acs.bioconjchem.9b00560 - Shinchi H., Yuki Y., et al., Glyco-Nanoadjuvants: Sugar Structures on Carriers of a Small
Molecule TLR7 Ligand Affect Their Immunostimulatory Activities.
ACS Appl. Bio Mater. 4(3), 2732-2741 (2021)
doi.org/10.1021/acsabm.0c01639 - Shinchi H., Komaki F., et al., Glyco-Nanoadjuvants: Impact of Linker Length for Conjugating a
Synthetic Small-Molecule TLR7 Ligand to Glyco-Nanoparticles on Immunostimulatory Effects
ACS Chem. Biol. 17(4), 957-968 (2022)
doi.org/10.1021/acschembio.2c00108 - TLRリガンド固定化ナノ粒子 [特許第7023460号], 隅田 泰生, 新地 浩之, 若尾 雅広, 登録日: 2022年2月14日
人工合成TLR9リガンドを用いた糖鎖ナノアジュバント
TLR9は、TLR7と同様に免疫細胞内のエンドソームに存在し、ウイルスが持つ一本鎖DNA (非メチル化CpGオリゴデオキシヌクレオチド: CpG ODN) を感知して自然免疫を活性化します。これまでに、TLR9を活性化する多様な人工合成CpG ODNが開発されており、その中でもCpG ODN 1018は、B型肝炎ワクチン (HEPLISAV-B) のアジュバントとして2017年に米国で臨床利用が承認されました。さらに、がん免疫療法への応用も検討されています。一方で、天然型のCpG ODNは、生体内で分解されやすいことが課題です。また、分解耐性を高める目的でDNAを繋ぐホスホジエステル結合をホスホロチオエート結合へ改変すると、非特異的な組織吸着の増加に伴う薬物動態の変化や副作用の発現が指摘されています。
そこで私たちは、α-マンノースを修飾した金ナノ粒子を人工合成CpG ODNのキャリアとして用いた『TLR9標的型糖鎖ナノアジュバント』を開発しました。
本技術により、天然型CpG ODNの分解耐性が向上し、さらに免疫細胞への送達効率も高まった結果、特に細胞性免疫の誘導活性を有意に向上させることに成功しました。
現在、他の糖鎖ナノアジュバントとの併用によりアジュバント活性をさらに高める研究を進めています。
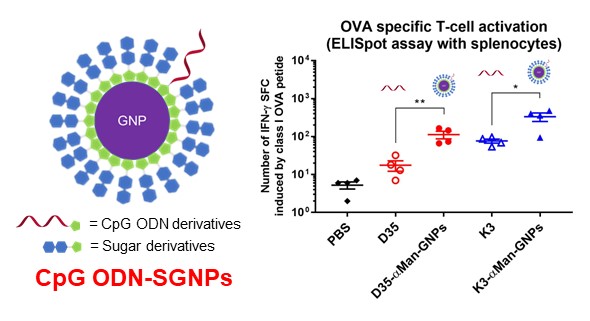
図. TLR9リガンド(CpG ODN)とα-マンノースを共固定化した金ナノ粒子
<関連論文>
- Murata K., et al., Improvement of the Nuclease Resistance and Immunostimulatory Activity of CpG Oligodeoxynucleotides by Conjugation to Sugar-Immobilized Gold Nanoparticles.
Bioconjugate Chem. 35(6), 804-815 (2024)
doi.org/10.1021/acs.bioconjchem.4c00145
合成低分子TLR4リガンドを用いた糖鎖ナノアジュバント
TLR4は、免疫細胞の細胞表層に多く存在し、細菌由来のリポ多糖 (LPS) を感知して自然免疫を活性化します。
これまでに、モノホスホリルリピドA (MPLA) などの人工リガンドが開発され、MPLAは子宮頸がんワクチンのアジュバントとして臨床利用されています。
一方で、ワクチン抗原の免疫原性を高めるにはアジュバント分子との複合化が重要と考えられていますが、薬物活性を保持したまま簡便に抗原分子などと複合化可能な合成低分子TLR4リガンドは、依然として開発途上にあります。
そこで私たちは、合成低分子TLR4リガンドの構造最適化を行い、免疫刺激活性を保持しつつ多様な分子と複合化できる新規合成低分子TLR4リガンドを開発しました。そして、この人工合成TLR4リガンドを用いて糖鎖修飾金ナノ粒子と複合化した『TLR4標的型糖鎖ナノアジュバント』を開発しました。TLR4リガンドは、TRIF経路を介して長期間持続する免疫応答を誘導すると考えられています。このことから、現在、他の糖鎖ナノアジュバントとの併用により長期間持続する免疫応答を誘導可能なアジュバントの開発に関する研究を進めています。
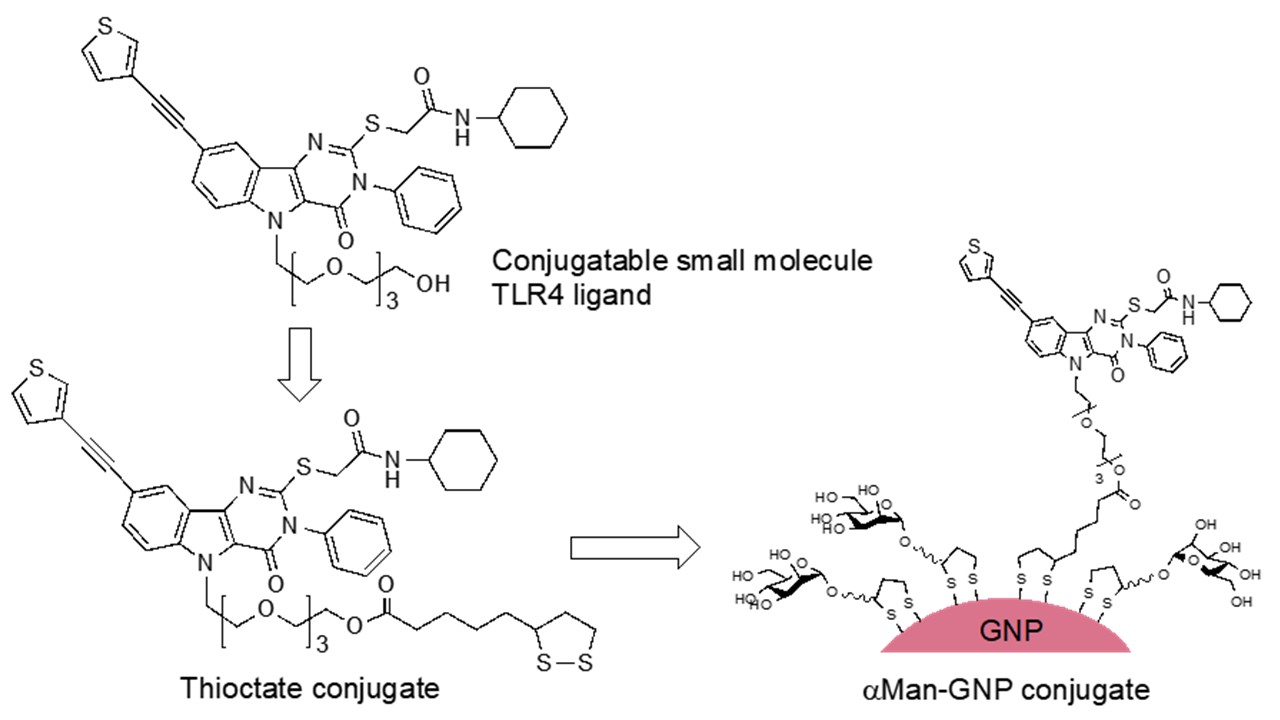
図. 構造最適化された低分子TLR4リガンドとα-マンノースを共固定化した金ナノ粒子
<関連論文>
- Mahara Y.,et al., Design and Application of Conjugatable Small Molecule Toll-like Receptor 4 Ligands
Bioconjugate Chem. 36(7), 1409-1420 (2025)
doi.org/10.1021/acs.bioconjchem.5c00076