研究内容
研究内容①:次世代アジュバントの開発とワクチン・免疫療法への応用
アジュバントとは、免疫応答を増強する物質の総称です。感染症ワクチンでは、抗原だけでは十分な免疫反応が得られない場合が多く、その効果を補完・増強する目的で用いられます。近年では、免疫機能の調節を通じて、がんやアレルギーを治療する免疫療法への応用も広がっています。しかし、現在使用されている多くのアジュバントは、抗体を産生する「液性免疫」の強化に偏っており、ウイルス感染細胞やがん細胞の排除に重要な「細胞性免疫」を十分に誘導できないという課題があります。
この問題に対し、当研究室では、免疫細胞を活性化する『Toll様受容体 (TLR)』を標的とした次世代アジュバントの開発に取り組んでいます。TLRは免疫細胞に多く存在し、ウイルスや細菌などの病原体由来分子を感知して自然免疫を起動する受容体群です。近年、TLRを活性化する人工合成リガンドが数多く開発され、感染症ワクチンや免疫療法のアジュバントとして注目されています。一方で、生体内での薬効の低さや副反応の問題が、実用化の大きな障壁となっています。
そこで私たちは、多彩な生物学的機能を持つ『糖鎖』の特性に着目し、これを利用してTLRリガンドを免疫細胞へ選択的かつ効率的に送達する新規アジュバントの開発に取り組んでいます。具体的には、糖鎖そのもの、あるいは糖鎖修飾金ナノ粒子 (SGNP) とTLRリガンドを複合体化し、薬効の増強と副反応の低減について検討しています。こうして得られた低・中分子型およびナノ粒子型の「糖鎖修飾アジュバント」は、液性免疫に加えて細胞性免疫も強力に誘導できることが示されており、現在、感染症ワクチンやがん免疫療法への応用を目指した研究を展開しています。
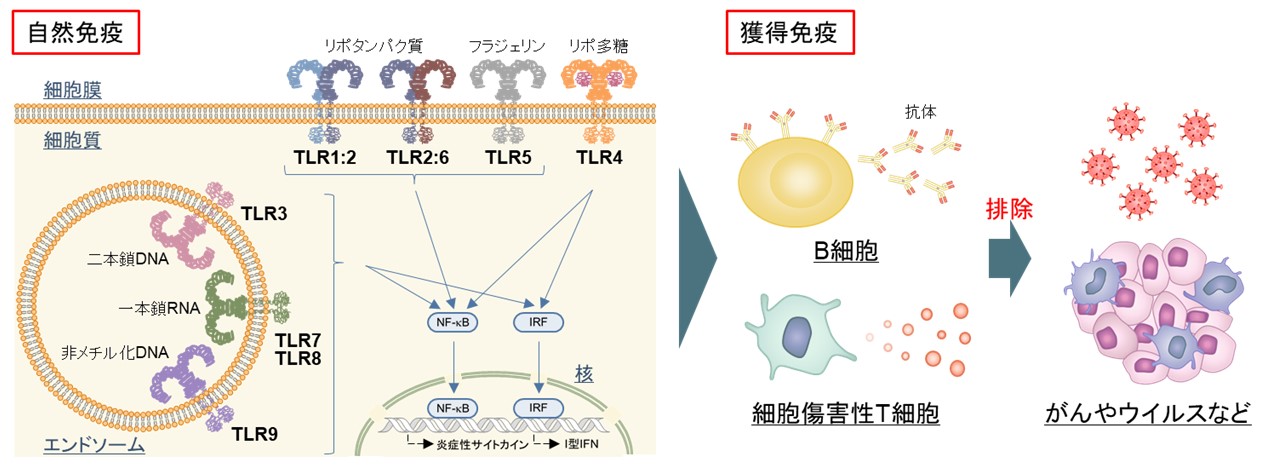
図. TLRが認識する分子とTLRの活性化によって誘導される免疫応答
研究内容の詳細
研究内容②:糖鎖の機能解明に向けた化学合成法・相互作用解析手法の開発
糖鎖は、DNAやタンパク質と並ぶ生命の主要な構成要素であり、すべての細胞表面に存在します。その機能は多岐にわたり、細胞間の情報伝達や免疫応答の制御に加え、ウイルスや細菌の感染にも深く関与しています。さらに、細胞表面に発現する糖鎖受容体は、外来異物の認識や糖タンパク質の品質管理に重要な役割を担い、細胞種ごとに異なる糖鎖認識機構を備えています。このような特性から、糖鎖を薬物送達システムの標的指向性分子として活用する研究が進められています。また、糖鎖の構造や発現量は、疾患や炎症などの生体内の状態変化に応じて大きく変動することから、がん細胞の識別や疾患診断のバイオマーカー (目印) としての応用が期待されています。
一方、糖鎖は化学構造が複雑で、天然由来の特定構造を選択的に単離することが難しく、その機能が十分に解明されていないものも多く存在します。そのため、構造が明確な糖鎖を化学的に合成し、それを用いて精密な機能解析を行うことが不可欠です。さらに、糖鎖–タンパク質間相互作用では、一価の糖鎖では結合が弱く、糖鎖が集合して多点で相互作用する「クラスター効果」が重要になります。したがって、糖鎖–タンパク質間の結合様式や結合強度を精密に評価することは容易ではありません。
そこで私たちは、これらの課題を解決するために、糖鎖の化学合成法を開発するとともに、糖鎖–タンパク質間の相互作用を適切に再現・評価できる新規結合性解析手法を確立し、糖鎖機能の分子レベルでの解明を目指しています。
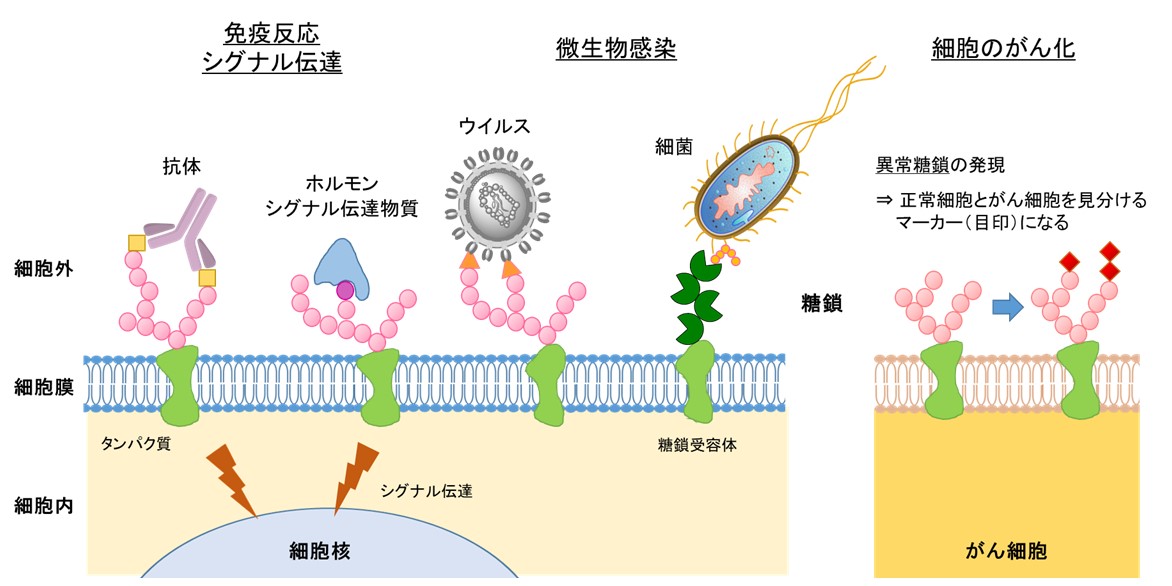
図. 糖鎖が関与する生命現象