研究内容
糖鎖の化学合成法の開発
研究背景
細胞表層に発現する糖鎖は、タンパク質や脂質に結合し、糖タンパク質やプロテオグリカン、糖脂質として存在しています。 その中でもプロテオグリカンは、糖鎖の中でも最も構造が複雑な硫酸化多糖のグリコサミノグリカン(GAG)を持っています。 GAGは、糖鎖構造をもとに分類されており、ヘパラン硫酸 (HS) やコンドロイチン硫酸 (CS)、ケラタン硫酸 (KS)、デルマタン硫酸 (DS) などがあります。 細胞外マトリックスの主要な構成成分であり、細胞の接着や増殖、分化、細胞の機能や形態の維持など、組織を形成する上で重要な働きを担っています。 近年、このGAGの微細構造が成長因子やケモカインなどの生理活性分子との相互作用に重要であることが示唆されており、その分子レベルでの解析が重要視されています。 しかしながら、GAGの糖鎖構造は非常に複雑であり、天然から特定の構造のみを単離することが極めて困難です。 そのため、未だに分子レベルでの機能解明には至っておらず、化学的に合成した構造明確なGAG鎖を用いた詳細な機能解析が求められています。

図. プロテオグリカンの生理機能(左)とGAGの構造の例(右)
グリコサミノグリカン (GAG) 部分糖鎖構造のライブラリー化
GAGと生理活性分子との相互作用を分子レベルで解析するために、HS や CS、KS、DS の部分糖鎖構造の化学合成を行っています。 糖鎖の合成においては、さまざまな硫酸化パターンの糖鎖を合成できるような中間体(ビルディングブロック)をデザインし、共通中間体から誘導されたGAG部分糖鎖構造のライブラリー化を進めています。 合成した糖鎖は、リンカー化合物を修飾後、表面プラズモン共鳴(SPR)法を用いて、さまざまな生理活性タンパク質との相互作用解析に利用することができます。 現在は、GAG部分構造のライブラリー化を進めるとともに、細胞増殖因子や成長因子をはじめとする様々な生理活性タンパク質との構造活性相関解析を行い、GAGの関与する生体機能の解明を行っています。
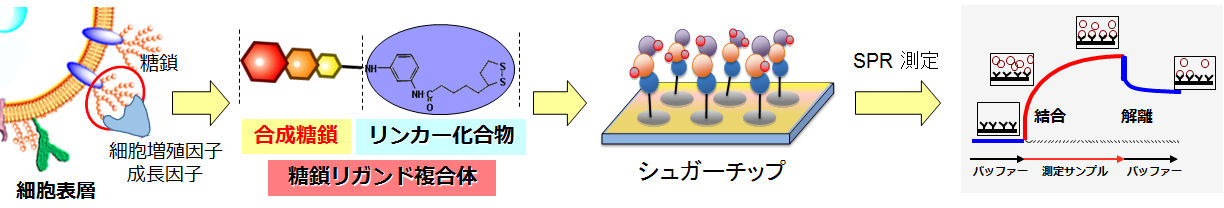
図. GAG部分糖鎖構造を固定化したシュガーチップを用いたSPR解析
<関連論文>
- Wakao M., et al., Sugar Chips immobilized with synthetic sulfated disaccharides of
heparin/heparan sulfate partial structure.
Bioorg. Med. Chem. Lett. 18, 2499-2504 (2008)
doi: 10.1016/j.bmcl.2008.01.069 - Saito A., et al., Towards the assembly of heparin and heparan sulfate oligosaccharide
libraries: efficient synthesis of uronic acid and disaccharide building blocks.
Tetrahedron 66, 3951-3962 (2010)
doi: 10.1016/j.tet.2010.03.077 - Wakao M., et al., Synthesis of a chondroitin sulfate disaccharide library and a GAG-binding
protein interaction analysis.
Bioorg. Med. Chem. Lett. 25, 1407-1411 (2015)
doi: 10.1016/j.bmcl.2015.02.054 - Miyachi K., et al., Syntheses of chondroitin sulfate tetrasaccharide structures containing
4,6-disulfate patterns and analysis of their interaction with glycosaminoglycan-binding protein.
Bioorg. Med. Chem. Lett. 25, 1552-1555 (2015)
doi:10.1016/j.bmcl.2015.02.054 - Kakitsubata Y., et al., Toward the construction of dermatan sulfate (DS) partial disaccharide
library: efficient synthesis of building blocks, common intermediate, and ligand conjugate of type-B DS
disaccharide.
Tetrahedron Lett., 57, 1154-1157 (2016)
doi:10.1016/j.tetlet.2016.01.105