研究内容
糖鎖リガンド複合体を利用した糖鎖結合性分子との相互作用解析ツールの開発
金属基盤に簡便に固定化可能な糖鎖リガンド複合体
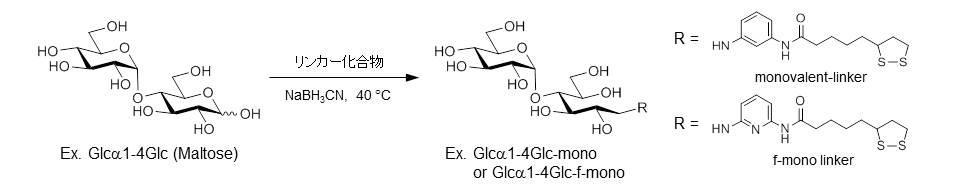
当研究室では、糖鎖と糖鎖結合性分子との相互作用解析に利用する糖鎖リガンド複合体を開発しました。糖鎖リガンド複合体は、ジスルフィド基を有する独自開発のリンカー化合物 (monovalent-linker または f-mono linker) が複合化されており、金属原子と硫黄原子の高い親和性を利用することで、相互作用解析に利用するための様々な金属基盤に簡便に糖鎖を固定化できます。通常、糖鎖にチオール基やアミノ基などの反応性官能基を導入するためには、複雑な化学反応を行わねばならず、硫酸化糖鎖などはその過程で硫酸基などが欠落する恐れがあります。一方、我々のリンカー化合物は、還元アミノ化反応による穏やかな条件で糖鎖と縮合させるため、糖に結合している官能基に全く影響を与えることなく、簡便に複合化することができます (図1)。糖鎖リガンド複合体の精製においても、monovalent-linkerは紫外吸収を、f-mono linkerは蛍光を利用して検出できるため、逆相カラムクロマトグラフィーにより反応生成物を容易に精製することができます。糖鎖リガンド複合体は、下記に示す様々な解析ツールに利用されており、隅田研究室のコア技術となっています。
<関連論文>
Suda Y., et al., Immobilization and clustering of structurally defined oligosaccharides for sugar chips: an improved method for surface plasmon resonance analysis of protein-carbohydrate interactions.
Bioconjug. Chem. 2006, 17, 1125-1135. doi: 10.1021/bc0600620
Sato M., et al., High-sensitivity analysis of naturally occurring sugar chains, using a novel fluorescent linker molecule.
J. Biochem. 2009, 146, 33-41. doi: 10.1093/jb/mvp041
糖鎖結合性分子との相互作用をリアルタイムに解析可能なシュガーチップ
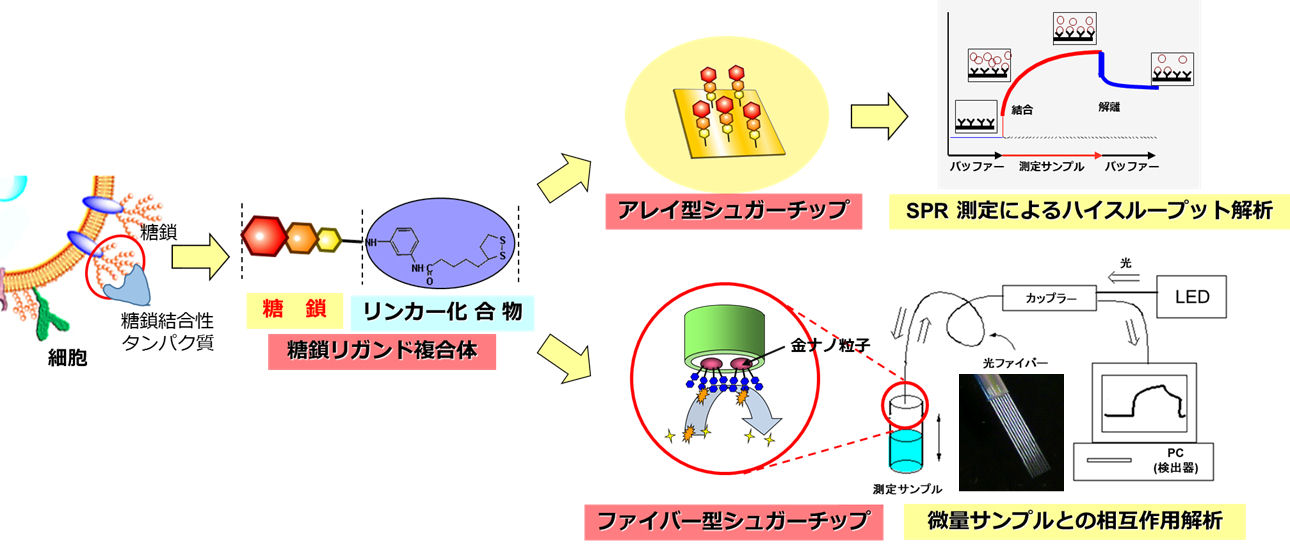
糖鎖と糖鎖結合性分子との相互作用をリアルタイムに解析するツールとして、アレイ型とファイバー型の2種類のシュガーチップの開発しました (図2)。これらのシュガーチップは、表面プラズモン共鳴(SPR)または局在プラズモン共鳴(LPR)を利用したバイオセンサーのセンサーチップとして利用することができ、糖鎖結合性分子との相互作用を無標識下でリアルタイムに解析することができます。アレイ型シュガーチップの特徴は、最大96種類の糖鎖を固定化できることであり、糖鎖とタンパク質間の相互作用を一挙に解析できます。当研究室では糖鎖の化学合成にも取り組んでおり、硫酸化糖鎖をはじめとする様々な糖鎖ライブラリーを有しています。これらを利用することで、構造が明確でより微細な構造に対する糖鎖結合性分子との相互作用が可能です。一方、ファイバー型シュガーチップは、微細な光ファイバー先端を利用し、その端面に金ナノ粒子を介して糖鎖を固定化したチップです。10 μL程度の微量なサンプル量でも、一般的なSPRバイオセンサーと同等の感度で相互作用を解析できることが特徴です。現在は、これらのシュガーチップを利用して、疾患特異的に発現する糖鎖に対する分子標的薬の探索を行っています。
<関連論文>
Suda Y., et al., Immobilization and clustering of structurally defined oligosaccharides for sugar chips: an improved method for surface plasmon resonance analysis of protein-carbohydrate interactions.
Bioconjug. Chem. 2006, 17, 1125-1135. doi: 10.1021/bc0600620
Wakao M., et al., Optical Fiber-Type Sugar Chip Using Localized Surface Plasmon Resonance.
Anal. Chem. 2017, 89, 1086-1091. doi:10.1021/acs.analchem.6b02380
糖鎖結合性分子との相互作用を簡便に解析可能な糖鎖固定化ナノ粒子
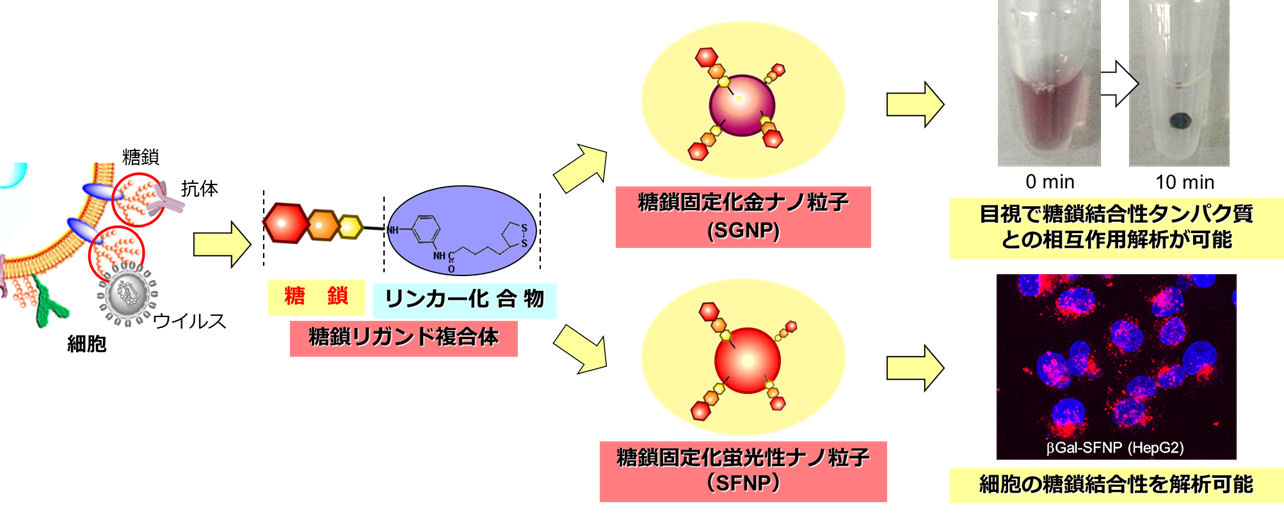
生体内に存在する糖鎖は、糖鎖同士や特定のタンパク質との相互作用を介して様々な生体現象に関与することから、糖鎖構造と機能の相関解析は現在でも重要な研究テーマの一つです。一方、糖鎖-糖鎖間または糖鎖-タンパク質間の相互作用は、タンパク質同士の相互作用に比べると非常に弱いため、その相互作用を解析することがしばしば困難になります。糖鎖の結合性を向上させる方法の一つとして、「糖鎖クラスター効果」を利用する方法があります。この方法では、糖鎖を集合化(クラスター化)することによって見かけの糖鎖結合性を向上させることができます。我々は、金ナノ粒子や量子ドットなどの様々な金属ナノ粒子(5~50 nm程度、nm=1 mmの100万分の1)の表面に糖鎖を高密度に固定化した糖鎖固定化ナノ粒子を開発しました。ナノ粒子上に固定化する糖鎖は、独自開発したリンカー化合物を用いることで自由に選択することができ、一個のナノ粒子表面に複数種類の糖鎖を固定化することも可能です。これらのナノ粒子は、糖鎖結合性分子との親和性が高くなり、凝集反応により相互作用を目視で解析できるため、糖鎖との相互作用を簡便に解析することができます (図3)。また、ナノ粒子に量子ドットを用いた場合、その蛍光性を利用することで、有機蛍光色素を修飾した糖鎖では解析が困難な細胞表層の糖鎖受容体の解析などにも利用可能です (図3右下)。現在は、これらを応用し、感染症などの疾患の診断に利用する研究も展開しています。
<関連論文>
Nakamura-Tsuruta S., et al., One-Step purification of lectins from banana pulp using sugar-immobilized gold nano-particles (SGNPs).
J. Biochem. 2008, 143, 833-839. doi: 10.1093/jb/mvn038
Shinchi H., et al., Stable sugar-chain-immobilized fluorescent nanoparticles for probing lectin and cells.
Chem. Asian J. 2012, 7, 2678-2682. doi: 10.1002/asia.201200362
Shinchi H., et al., Cadmium-free sugar-chain-immobilized fluorescent nanoparticles containing low-toxicity ZnS-AgInS2 cores for probing lectin and cells.
Bioconjug. Chem. 2014, 25, 286-295. doi:10.1021/bc400425w